
如下图所示,在一片高致密的氧化锆固体电解质的两侧,用烧结的方法制成几微米到几十微米厚的多孔铂层作为电极,再在电极上焊上铂丝作为引线,就构成了氧浓差电池。如果电池左侧通入参比气体(空气),其氧分压为P0;电池右侧通入被测气体,其氧分压为P1。
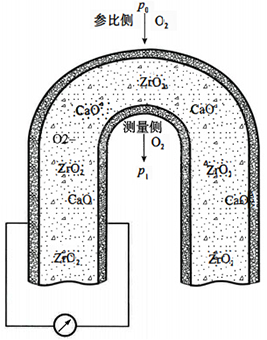
设P0>P1,在高温下(650~850℃),氧就会从分压大的P0侧向分压小的P1侧扩散,这种扩散,不是氧分子透过氧化锆从P0侧到P1侧,而是氧分子电离成氧离子后通过氧化锆的过程。在750℃左右的高温中,在铂电极的催化作用下,在电池的P0侧发生还原反应,一个氧分子从铂电极取得4个电子,变成两个氧离子(O2-) 进入电解质,即:
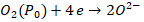
P0侧的铂电极由于大量给出电子而带正电,成为氧浓差电池的正极或阳极。
这些氧离子进入电解质后,通过晶体中的空穴向前运动到达右侧的铂电极,在电池的P1侧发生氧化反应,氧离子在铂电极上释放电子并结合成氧分子析出,即:
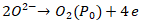
P1侧的铂电极由于大量得到电子而带负电,成为氧浓差电池的负极或阴极。
这样在两个电极上由于正负电荷的堆积而形成一个电势,称之为氧浓差电动势。当用导线将两个电极连成电路时,负极上的电子就会通过外电路流到正极,再供给氧分子形成氧离子,电路中就有电流通过。
氧浓差电动势的大小,与氧化锆固体电解质两侧气体中的氧浓度有关。通过理论分析和试验证实,它们的关系可用能斯特方程式表示:
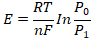
式中E为氧浓差电动势,V;R为气体常数,8.315J/(mol·K);T为气体的绝对温度,273+t(t为实际工作温度,℃ );F为法拉第常数,96500C/mol;n为参加反应的电子数(对氧而言,n=4);P0为参比侧的氧分压;P1被测气体的氧分压。
如被测气体的总压力与参比气体的总压力相同,则上式可改写为:
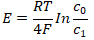
式中c0为参比气中氧的体积分数;c1为被测气体中氧的体积分数。
从上式可以看出,当参比气体中的氧含量c0一定时,氧浓度差电动势仅是被测气体中氧含量c1和温度T的函数。把上式的自然对数换为常用对数,得
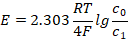
若氧浓差电池的工作温度为750℃, c0为20.8%,则电池的氧浓差电动势E为
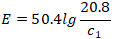
公式
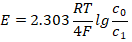 说明,浓差电动势与被测气体中氧含量有对数关系,当氧浓差电池的工作温度T和参比气体中氧含量c0一定时,被测气体中的氧含量越小,氧浓差电动势越大。这对于测量氧含量低的烟气是有利的,但是在自动控制系统中,需要有线性化装置来修正对数输出特性。
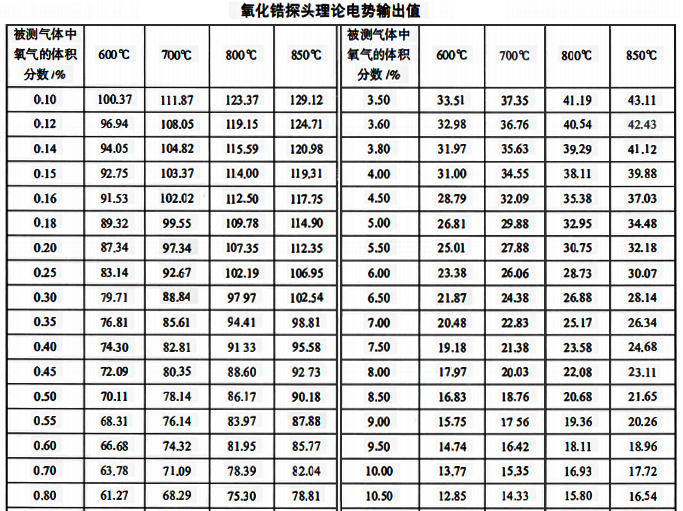
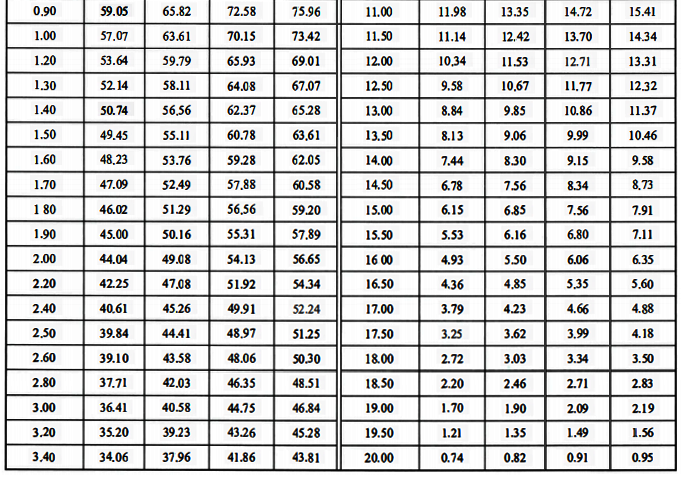
说明,浓差电动势与被测气体中氧含量有对数关系,当氧浓差电池的工作温度T和参比气体中氧含量c0一定时,被测气体中的氧含量越小,氧浓差电动势越大。这对于测量氧含量低的烟气是有利的,但是在自动控制系统中,需要有线性化装置来修正对数输出特性。按式公式计算得出的氧化锆探头理论电势输出值见下表。
相关阅读
◆氧化锆氧量分析仪十问十答
◆三张图弄懂氧化锆氧量分析仪典型系统配置
◆如何进行氧化锆氧量分析仪标定方法及参数设置








