摩尔浓度:溶液中溶质物质的量/溶液的体积。常见的单位为mol/L。我们简单的举例,计算下两者之间的换算:g/L和mol/L之间的换算。分母都是L,暂且不管。只要将g换算成mol即可。
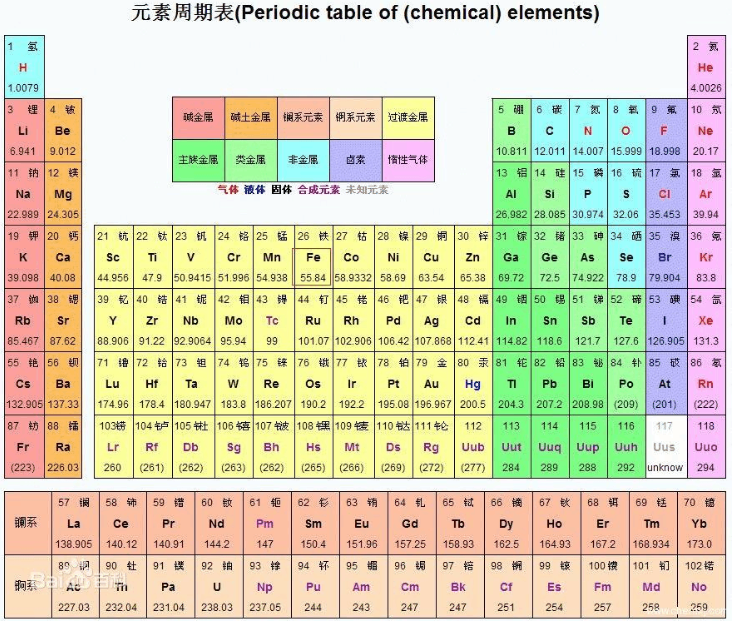
物质的量=质量/原子量或分子量。元素的原子量,可以查阅元素周期表。
这是最简单的换算,有时候需要将质量换算成体积,然后再换算成物质的量浓度。摩尔浓度和质量浓度之间的换算公式可以参考下面的公式:
ρ=m/v=nMr/v=(n/v)Mr=cMr
其中,ρ代表质量浓度,m代表质量,v代表体积,n代表溶质的物质的量,Mr代表溶质的摩尔质量,c代表物质的量浓度。
还有一个重要的常数需要大家记住,那就是阿伏加德罗常数。
1mol任何粒子所含的粒子数均为阿伏加德罗常数。阿伏加德罗常数的近似值为:6.02×10²³mol-1。阿伏加德罗常数之所以伟大,是因为它给了我们一个恒定的量:在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子。阿伏加德罗常数是联系微观世界和宏观世界的桥梁。
几种概念我们再梳理一下:摩尔质量=物质的相对原子(分子)质量;阿伏伽德罗常数×物质的量=微粒数;质量=摩尔质量×物质的量




